 Blog
Blog
Powrót do listy
Insulina - zobacz, jak działa! 6 faktów, które musisz znać!
09 czerwca 2020
Panująca moda na dietę niskowęglowodanową wygenerowała szereg mitów, a ponieważ insulina jest hormonem, który odgrywa ważną rolę w metabolizmie cukrów, musiało się jej oberwać. Insulina została obwiniona o epidemię otyłości w XXI wieku. Czy faktycznie insulina odpowiada za to, że Twój ptaszek ma nie tylko daszek, ale i właściciela zagrożonego cukrzycą typu II?
Spis treści
- Insulina wydziela się tylko w okolicach posiłków
- Insulina zmniejsza apetyt
- Insulina wzrasta po spożyciu białka
- Skoki insuliny
- Insulina i tłuszcze
- Insulina i glukoza
- Nie tyjesz od insuliny
- Podsumowanie
Insulina wydziela się tylko w okolicach posiłków
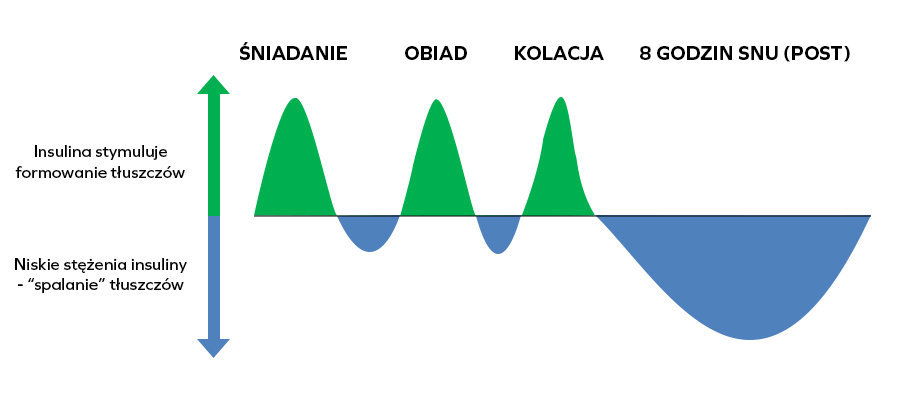
Moda na diety niskowęglowodanowe opiera się na wielu domysłach i przypuszczeniach. Jednym z błędnych założeń jest przeświadczenie, że insulina w przebiegu diety wysokowęglowodanowej osiąga niebezpiecznie długo utrzymujące się, wysokie stężenia. Oznacza to zahamowanie lipolizy i wzrost lipogenezy – zaczynasz tyć!
Pogadajmy o faktach. U zdrowych osób insulina rośnie tylko po spożyciu pokarmu. Pomiędzy posiłkami insulina zmniejsza swoje stężenie. Mówiąc po ludzku - po posiłku Twój organizm odłoży trochę tłuszczyku. Jednakże w przerwie pomiędzy kolejnymi posiłkami wykorzysta go na bieżące potrzeby. Jeśli w ciągu doby dostarczysz mniej kalorii niż wydatkujesz – schudniesz. Pewnym potwierdzeniem są mieszkańcy wyspy Okinawa. Słyną oni z długowieczności i niewielkiego odsetka osób otyłych, mimo wysokiego udziału węglowodanów w swojej diecie [1].
Potrzebujesz konsultacji z dietetykiem? Przestań się dręczyć i oddaj się w ręce specjalisty. Pomogliśmy ponad 20 000 osób osiągnąć cel, a nasza opinia w Google to 5/5 na podstawie ponad 390 opinii. Szybkie, smaczne i indywidualne diety online to nasza specjalność.
Insulina zmniejsza apetyt
Wiecie skąd wzięło się przeświadczenie, że insulina zwiększa apetyt? Internetowi szamani rozgłaszali takie nowiny na podstawie badań, w których wstrzykiwano samą insulinę, bez dostarczenia kalorii. To ma oczywisty efekt – hipoglikemia (zbyt niskie stężenie cukru we krwi) i pojawienie się głodu. Nie jest to jednak odzwierciedlenie sytuacji, która spotka Cię przy śniadaniu. Chyba, że bawisz się na czczo w pielęgniarkę :)
Zjedzenie posiłku obfitującego w węglowodany zmniejsza apetyt. Udowodniono, że podanie insuliny do mózgu hamuje apetyt. Wykazano nawet, iż uszkodzenie receptorów dla insuliny w mózgu gryzoni powoduje, że zwierzęta zaczynają się przejadać (nie czują sytości). Oczywiście wpływ na to, jak długo będziesz syty po posiłku, ma wiele czynników. M.in. zawartość białka i tłuszczów, ładunek glikemiczny czy obecność błonnika w posiłku. Mimo wszystko, wiele eksperymentów wykazało, że insulina doskonale zmniejsza apetyt [2, 3].
Insulina wzrasta po spożyciu białka
Insulina silnie reaguje na spożycie spożycie białka. Co ciekawe, nie jest to związane ze zmianami cukru we krwi czy glukoneogenezą (proces, w którym Twoja wątroba pozyskuje glukozę m.in z białka). Aminokwasy mogą bezpośrednio stymulować trzustkę do produkcji insuliny. Sztandarowym przykładem jest leucyna [4]. Im jej więcej w posiłku – tym więcej insuliny. Białko pobudza również wydzielenie glukagonu (hormon antagonistyczny w stosunku do insuliny, stymuluje wzrost stężenia glukozy we krwi). Nie myśl jednak, że dzięki temu możesz palić tłuszcz, podczas gdy we krwi znajduje się sporo insuliny. Glukagon nie zwiększa lipolizy u ludzi [5]. Stymulując wątrobę, sprawia jednak, że insulina, która zostaje pobudzona przez białko, nie obniża drastycznie stężenia glukozy we krwi. Holenderscy naukowcy wykazali, iż insulina może zostać pobudzona w większym stopniu posiłkiem wysokobiałkowym niż wysokowęglowodanowym [6].
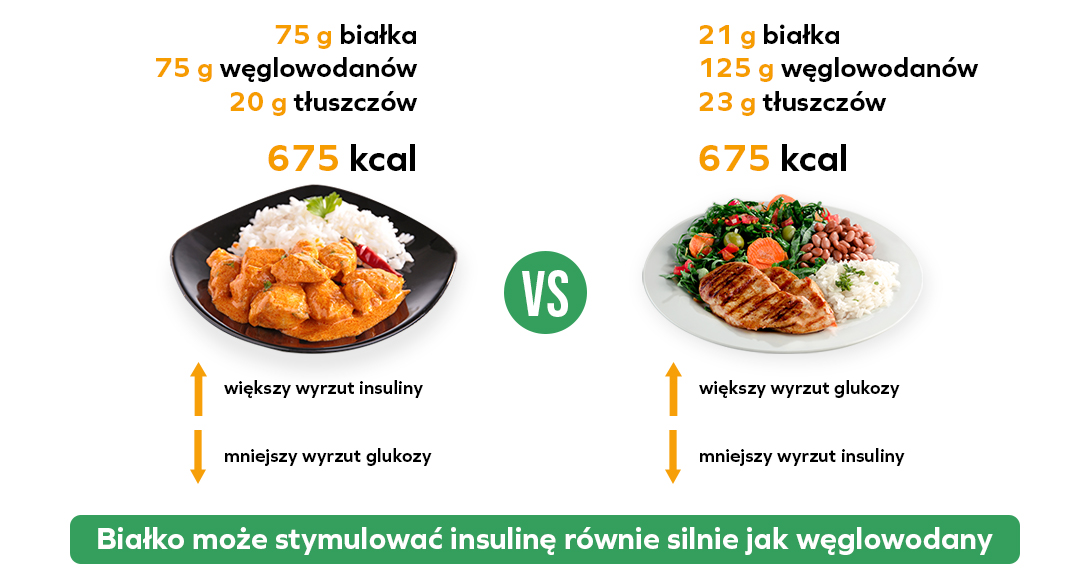
Insulina najmocniej stymulowana jest przez białko serwatkowe (białko mleka). Za nimi znajdują się ryby, drób i jajka. Dodatkowo, popularna serwatka syci bardziej niż inne źródła białka. Jednak to już ustaliliśmy, prawda? Insulina doskonale tłumi apetyt. Im jej więcej, tym większa sytość.
Skoki insuliny
Wydzielanie insuliny z trzustki występuje w dwóch fazach. Pierwsza z nich przebiega gwałtownie. Trzustka już ~2 minuty od momentu wzrostu stężenia cukru we krwi uwalnia insulinę. Trwa to około 10 minut. Druga faza trwa tak długo, jak wzrasta stężenie glukozy. Uwolniona zostaje zmagazynowana insulina oraz wytwarzana na bieżąco z prekursora zwanego proinsuliną [7]. U zdrowych osób „skoki” insuliny są normalne. Co ciekawe, w przypadku osób z zaburzoną tolerancją glukozy, pierwszy, gwałtowny skok insuliny ulega upośledzeniu. To oznacza, że „skoki” insuliny to standardowa, fizjologiczna reakcja organizmu. Oczywiście mowa tutaj referencyjnych wyrzutach insuliny, nie hiperinsulinemii (czyli jej zbyt wysokim poziomie).
Świetnym przykładem, tonującym obawy wobec insuliny, jest białko. Ten makroskładnik powoduje gwałtowne skoki insuliny, jednakże zmniejsza apetyt i przyczynia się do utraty wagi. Podobnie jak leki naśladujące glukagonopodobny peptyd-1 (glucagon-like peptide-1, GLP-1), które są stosowane w terapii cukrzycy typu 2 – nasilają wydzielanie insuliny, jednocześnie przyczyniając się do utraty masy ciała.
Insulina i tłuszcze
Możesz przytyć na diecie ketogenicznej. Tak, tłuszcz też idzie w tłuszcz. W Twoich komórkach tłuszczowych znajduje się enzym o mało ciekawej nazwie – lipaza hormonowrażliwa. Odpowiada za rozkład tłuszczów. Insulina hamuje jej aktywność, podobnie jak tłuszcz! To oznacza, że przejadanie się masłem i boczkiem… może pójść w boczki ;). Podobnie jak przejadanie się kaszą gryczaną. Możesz przytyć od każdego pokarmu, o ile przekroczysz swoje zapotrzebowanie energetyczne. Nie insulina jest za to odpowiedzialna, a Twoje obżarstwo! [8,9].
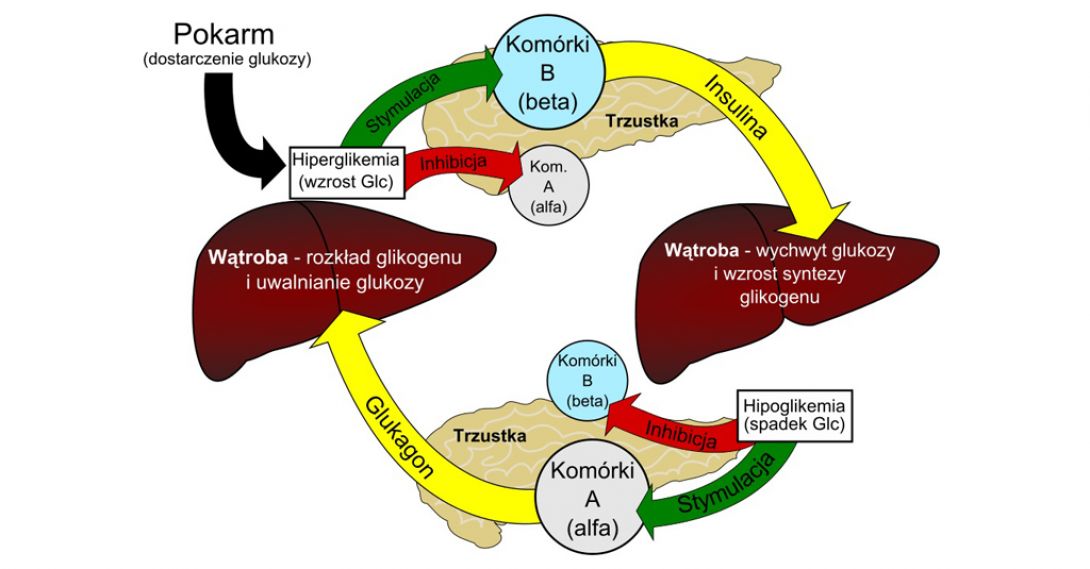
Insulina i glukoza
Glukoza pobierana jest do komórek poprzez grupę transporterów. Głównym jest GLUT-4. Insulina odpowiada za pobudzenie GLUT-4 do przemieszczenia się z wnętrza do powierzchni komórki, gdzie glukoza może związać się z nim i wejść do komórki. Jednakże, na powierzchni komórki znajduje się o wiele więcej transporterów glukozy, nawet w przypadku braku insuliny. Insulina zwiększa wchłanianie glukozy, nie jest jednak niezbędna do tego. Cukrzycy typu I nie charakteryzują się zwiększonym stężeniem glukozy we krwi ze względu na to, że glukoza nie ma możliwości dostania się do komórek. W rzeczywistości wychwyt glukozy przez komórki jest zwiększony, a konsekwencją braku insuliny jest wzmożona glukoneogeneza (tworzenie glukozy z innych źródeł niż węglowodany) oraz glikogenoliza (rozkład glikogenu wątrobowego). Tym samym, wysoki poziom cukru we krwi na czczo, jest spowodowany nadprodukcją glukozy z wątroby, a nie dlatego, że glukoza nie może dostać się do komórek. Podana insulina hamuje glukoneogenezę i glikogenolizę co reguluje stężenie glukozy we krwi.
Nie tyjesz od insuliny
Zapewne wspólnie zgodzimy się ze stwierdzeniem: „oczyszczone węglowodany mogą przyczyniać się do wystąpienia otyłości”. Wiele osób uważa, że jest to spowodowane gwałtownymi skokami insuliny. Jednak to nieprawda, ponieważ białko również stymuluje wydzielanie insuliny, jednak przyczynia się do utraty masy ciała. Problem leży gdzie indziej. Rafinowane węglowodany charakteryzują się wysoką gęstością energetyczną. Mówiąc po ludzku - w przetworzonych produktach można upchać wiele kalorii w niewielkim opakowaniu. Dodatkowo, tego typu produktu słabo sycą, z powodu szybkiego wzrostu, a następnie gwałtownego spadku stężenia glukozy we krwi. Po prostu łatwiej zjeść więcej bazując na rafinowanych węglowodanach. Kolejnym problemem jest zawartość innych makroskładników w produktach obfitujących w oczyszczone węglowodany. Słodycze to często mieszanka cukru i tłuszczów. Niestety, mamy słabość do tego typu mieszanek i łatwiej nam popłynąć z produktem obfitującym w połącznie obu tych makroskładników. To przetworzona żywność jest problemem, nie insulina. W ramach ciekawostki dodamy, iż spożywanie rafinowanych węglowodanów nie wpływa negatywnie na wrażliwość insulinową, o ile kontrolujesz spożycie kalorii [10].
Podsumowanie
Wiele osób może stwierdzić, że podane informacje dotyczą tylko i wyłącznie osób zdrowych. Nic bardziej mylnego. Na przykład białko przyczynia się do utraty masy ciała u cukrzyków, pomimo, że silnie stymuluje wydzielanie insuliny. Oczywiście hiperglikemia poposiłkowa (zbyt duże stężenie glukozy we krwi po posiłku) przyczynia się do zwiększonego utleniania tkanek, zapalenia i dysfunkcji śródbłonka. To oznacza, że źle kontrolowany cukrzyk jest bardziej narażony na choroby. Jednakże problemem nie jest insulina, a czynniki wpływające na to, że insulina nie działa poprawnie. Co musisz zrobić, jeśli masz problem z nadmierną masą ciała? Jedz więcej białka, warzyw, owoców czy orzechów i nie przejadaj się. Deficyt energetyczny to najlepszy „suplement” na poprawę wrażliwości insulinowej.
Piśmiennictwo
- Willcox, Bradley J., et al. "Caloric restriction, the traditional Okinawan diet, and healthy aging: the diet of the world's longest‐lived people and its potential impact on morbidity and life span." Annals of the New York Academy of Sciences 1114.1 (2007): 434-455.
- Austin, Juliana, and Daniel Marks. "Hormonal regulators of appetite." International journal of pediatric endocrinology 2009.1 (2008): 1-9.
- Pliquett, R. U., et al. "The effects of insulin on the central nervous system-focus on appetite regulation." Hormone and metabolic Research 38.07 (2006): 442-446.
- Yang J., Chi Y., Burkhardt B. i wsp.: Leucine metabolism in tegulation of insulin secretion from pancreatic beta cells. Nutr Rev 2010,68(5),270-279.
- Gravholt C., Moller N., Jensen M. i wsp.: Physiological levels of glucagon do not influence lipolysis in abdominal adipose tissue as assessed by microdialysis. J Clin Endocrinol Metab 2001,86(5),2085-2089.
- Boelsma E., Brink E., Stafleu A. i wsp.: Measures of postprandial wellness after single intake of two protein-carbohydrate meals. Appetite 2010,54(3),456-464.
- Wilcox, Gisela. "Insulin and insulin resistance." Clinical biochemist reviews 26.2 (2005): 19.
- Hall K.: A review of the carbohydrate–insulin model of obesity. EJCN 2017,71,323-326.
- Evans K., Clark M., Frayn K.: Effects of an oral and intravenous fat load on adipose tissue and forearm lipid metabolism. Am J Physiol 1999, 241-248.
- Black R., Spence M., McMahon R. i wsp.: Effect of eucaloric high- and low-sucrose diets with identical macronutrient profile on insulin resistance and vascular risk: a randomized controlled trial. Diabetes 2006,55(12),3566-3572.
